贵州药品洁净室设计规范
网站编辑 2022-10-01 20:05:02 11161阅读
药品生产环境的空气洁净度等级的确定仍需满足以下要求:
1当医疗洁净室(区域)有多个过程时,应根据生产过程要求采用相应的空气洁净度等级。层流手术室手术室是采用空气洁净技术对微生物污染采取程度不同的控制,达到控制空间环境中空气洁净度适于各类手术之要求;并提供适宜的温、湿度,创造一个洁净舒适的手术空间环境。由于手术室要严格控制低细菌数及低麻醉气体浓度,所以层流超净装置的稳定性是层流净化手术室的重要验收指标。洁净手术室按不同专科,手术间又可分为普外、骨科、妇产科、脑外科、心胸外科、泌尿外科。烧伤科、五官科等手术间。由于各专科的手术往往需要配置专门的设备及器械,因此,专科手术的手术间宜相对固定。无菌手术室已通过医药洁净检测中心检测,为万级洁净实验室。主要开展项目为:CIK细胞免疫治疗、DC-CIK免疫治疗、超级免疫粒细胞治疗等。空气调节系统必须可靠运行,采用先进技术,合理利用和节约能源与资源,保证环境的质量和安全,为实验人员提供所需要的温度和湿度,保障生物实验在安全的条件下进行,以确保实验结果得准确性。
2。在满足生产工艺要求的前提下,医用洁净室的气流组织形式应采用工作区局部或全室空气净化或工作区局部和全室空气净化相结合的形式。
医疗洁净室设计中的几个问题
1.洁净室设计不能满足生产的实际需要
对于新建洁净室工程或大型洁净室改造工程,业主一般会要求正规的设计院进行设计,而对于中小型洁净室工程,考虑到造价,业主一般会与工程公司签订合同,其中:设计工作将由工程公司承担。尽管国家标准(GB50073-2001,洁净厂房设计规范简称)已经颁布,但一些中小型净化工程公司仍然不能正确理解和应用上述设计规范。在测试过程中经常会发现以下问题。
2.混淆洁净室探测目的。
洁净室性能测试和评估工作是衡量洁净室完工时是否满足设计要求(验收测试)和洁净室正常工作状态(定期测试)的必要工作步骤。验收测试包括两个阶段:洁净室综合性能的完成调试和综合评估。一些新建的洁净室通常将这两个阶段结合起来,通常与完成验收阶段的调整测试结果,而不是综合性能测试结果,或综合性能综合测试,以取代完成验收阶段的调整测试。这是不可取的。这两个测试阶段的目的是不同的,测试的内容是不一样的。完成验收阶段的测试集中在调整上,可能会重复几次。这种类型的测试主要由施工单元进行。洁净室的综合性能评估在完成验收测试后进行,由合格且经验丰富的第三方承担。
3.洁净室运作中的问题
洁净室布局不合理,2间洁净室清洁工作不规范。
3部分单程到一些洁净室
在测试风速和气流清洁度时,经常会遇到风速很小,几乎为零,并且在同一100级区域的某些部分清洁度经常超过标准。
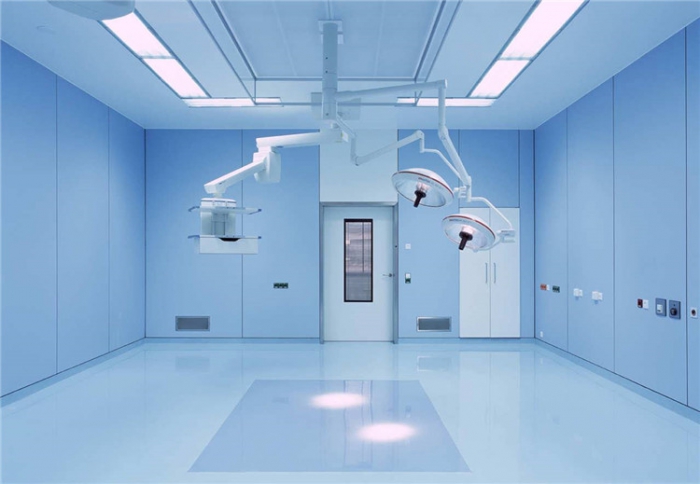

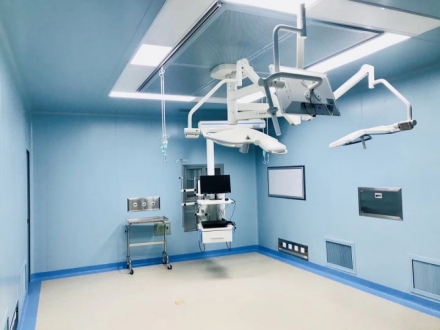 贵州手术室净化空调材料的选择
贵州手术室净化空调材料的选择